Analyse
Effets comparés des inhibiteurs des SGLT2 (gliflozines) et des antagonistes de l’aldostérone - surajoutés aux antagonistes du système rénine-angiotensine - sur la maladie rénale chronique des patients diabétiques de type 2
Contexte
Complication majeure du diabète de type 2, et important problème de santé publique, l’insuffisance rénale chronique a retenu l’attention de Minerva à plusieurs reprises. 3 groupes de médications ont été étudiés. En 2007, les inhibiteurs du système rénine-angiotensine- aldostérone montrent un effet protecteur supplémentaire (par rapport aux autres hypotenseurs) chez les patients présentant une albuminurie (1,2). Un effet favorable des gliflozines sur la progression de la maladie rénale diabétique, indépendamment de la maladie cardiovasculaire ou de la décompensation cardiaque (DC) se dégage progressivement, de 2016 à 2021 (3-8). Si les antagonistes de l’aldostérone (ARA) (stéroïdiens) sont reconnus actifs dans la DC (9,10), ces mêmes antagonistes stéroïdiens, et les récents ARA-non stéroïdiens apparaissent progressivement dans le paysage du traitement de l’insuffisance rénale du diabète (11). Pour les cliniciens, des essais comparant ces différentes (sous)-classes seraient évidemment bienvenus.
Résumé
Méthodologie
En l’absence d’essais avec comparaison directe, les auteurs présentent une méta-analyse en réseau (12).
Sources consultées
- PubMed, Embase, Central, jusqu’au 20/01/2022
- recherche manuelle d’études ou de méta-analyses relevantes via les articles inclus et dans Clinicaltrials.gov
- langue : uniquement en anglais.
Etudes sélectionnées
- critères d’inclusion : le bras « intervention » comporte soit une gliflozine (canagliflozine, dapagliflozine) soit un antagoniste du récepteur à l’aldostérone (ARA) stéroïdien (spironolactone, éplérénone) ou non stéroïdien (finérénone, exasérénone (ce dernier non commercialisé en Belgique)) ; le bras contrôle comporte soit un placebo, soit l’absence de traitement spécifique ; toute RCT précisant un critère de jugement prédéfini par les auteurs est incluse ; suivi minimum de 12 semaines
- au total : 16 RCTs ont été sélectionnées : 6 étudient les ARA non stéroïdiens (ARA-NSt), 4 les ARA stéroïdiens non sélectifs (ARA-NSel), 2 un ARA stéroïdien sélectif (éplérénone- ARA-Sel) et 4 une gliflozine (Glifz) ; le suivi moyen a été de 12 à 137 semaines
- 17 réseaux ont été analysés.
Population étudiée
- patients adultes (> 18 ans), diabétiques de type 2 avec IRC (stade 1 à 4)
- filtration glomérulaire supérieure à 15 ml/min/1,73 m²
- patients recevant un IEC ou un sartan
- ont été exclues les études avec patients dialysés, transplantés, ou dont le stade de l’insuffisance rénale chronique (IRC) n’était pas clairement établi
- au total, les données de 22981 patients ont été analysées ; l’âge moyen était de 64,1 ans (ET de 9,6 ans) ; la durée moyenne du diabète était de 15,1 ans et l’HbA1c était de 7,8% en moyenne (ET 1,4%) ; la GFR de 57,1 ml/min/1,73 m² (ET 21,1) ; la PA systolique moyenne de 138,3 mmHg (ET 15,2) et la PA diastolique moyenne de 77,4 mmHg (ET 13,9) ; 45.6% des patients présentaient un antécédent de maladie cardiovasculaire.
Mesures des résultats
- critère de jugement primaire :
- composite rénal (insuffisance rénale terminale, qui comprend dialyse/transplantation ou clearance < 15 ml/min/1,73 m², ou doublement de la créatinine sanguine ou mort de cause rénale)
- trois sous-analyses pour les 3 composantes du composite
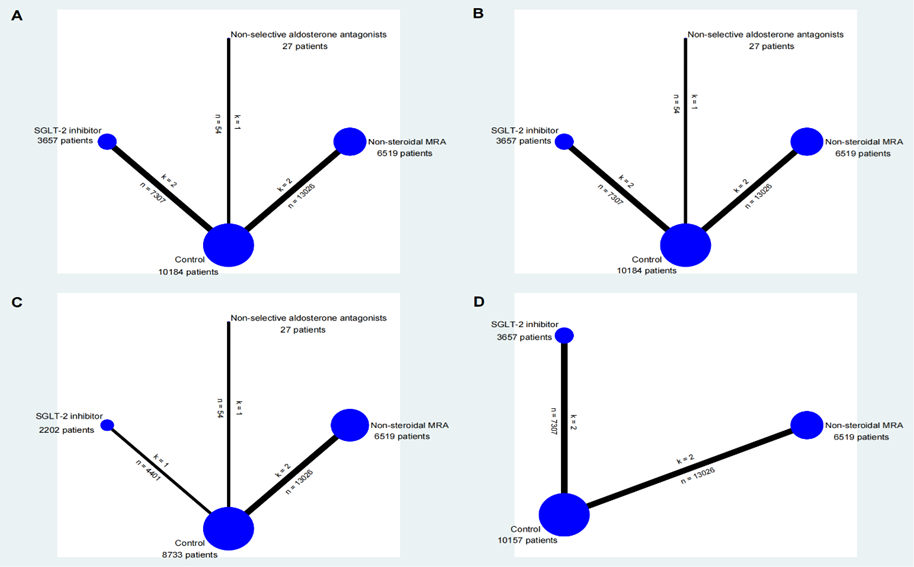
- pour la bonne compréhension du lecteur, l’architecture des réseaux analysés pour le composite primaire et ses composantes est présentée ici
Légende : A : critère de jugement primaire ; B, C, D : les 3 parties du composite ; k : nombre d’études ; n : nombre de patients
- critères de jugement secondaires : mort de cause cardiovasculaire (CV), infarctus myocardique non fatal, accident vasculaire cérébral non fatal, hospitalisation pour décompensation cardiaque (DC), mortalité toutes (TT) causes
- les résultats sont des OR avec leurs intervalles de crédibilité à 95% (statistiques bayésiennes) ; les résultats sont directs ou indirects.
Résultats
- critère de jugement primaire :
|
|
Composite |
Ins Rén Term |
Doubl Créat |
Mort Rénale |
|
Glifz / Contrôle |
0,62 (de 0,52 à 0,73) |
0,69 (de 0,57 à 0,83) |
0,60 (de 0,48 à 0,77) |
NS |
|
ARA-NSt / Contrôle |
0,76 (de 0,66 à 0,88) |
NS |
NS |
NS |
|
ARA-NSel/ Contrôle |
NS |
NS |
NS |
- |
ARA non stéroïdiens (ARA-NSt), ARA stéroïdiens non sélectifs (ARA-NSel) et gliflozine (Glifz) ; non significatif (NS)
-
- aucune comparaison indirecte n’est significative pour le critère de jugement primaire ou ses composantes
- critères de jugement secondaires :
|
|
Mortalité CV |
Hospitalisation DC |
Mortalité toutes causes |
|
Glifz/ Contrôle |
0,80 (de 0,65 à 0,98) |
0,57 (de 0,45 à 0,72) |
0,79 (de 0,66 à 0,93) |
|
ARA-NSt / Contrôle |
NS |
0,78 (de 0,66 à 0,92) |
NS |
|
ARA-NSel/ Contrôle |
- |
- |
NS |
ARA non stéroïdiens (ARA-NSt), ARA stéroïdiens non sélectifs (ARA-NSel) et gliflozine (Glifz) ; non significatif (NS)
-
- une seule comparaison indirecte est significative pour le critère hospitalisation pour DC (4 essais, 10176 patients) : gliflozines vs ARA-NSt : OR de 0,73 (avec ICr à 95% de 0,55 à 0,97)
- l’analyse des effets indésirables : les auteurs analysent les effets sur la TA syst (*: ne sont pas des OR, mais des différences moyennes pondérées), la TA diastolique, l’insuffisance rénale aigüe, la natrémie (hyponatrémie), la kaliémie (hyperkaliémie) et l’hypotension orthostatique (diminution du volume circulant); les résultats sont présentés avec leur IC à 95% :
|
|
TA syst |
Hyponatrémie |
Hyperkaliémie |
Hypo orthost |
|
Glifz / Contrôle |
-3,5 (de -1,01 à -6,01) * |
NS |
NS |
1,28 (de 1,06 à 1,56) |
|
ARA-NSt / Contrôle |
-10,96 (de -0,46 à -20,49) * |
16,56 (de 2,78 à 455,19) |
2,27(de 2,02 à 2,56) |
NS |
|
ARA-NSel/ Contrôle |
NS |
- |
3,22 (de 1,43 à 7,66) |
- |
|
ARA-Sel / Contrôle |
- |
- |
NS |
- |
ARA non stéroïdiens (ARA-NSt), ARA stéroïdiens non sélectifs (ARA-NSel), ARA stéroïdien sélectif (éplérénone- ARA-Sel) et gliflozine (Glifz) ; non significatif (NS), * : différence moyenne pondérée
-
- les comparaisons indirectes significatives sont :
- pour la TA syst : ARA-NSt/ARA-NSel : DMS de -10,37 (avec IC à 95% de -0,54 à -20,19)
- pour l’hyponatrémie : ARA-NSt/Glifz : OR de 23,81 (avec IC à 95% de de 2,04 à 888,94)
- pour l’hyperkaliémie : ARA-NSt/Glifz : OR de 2,73 (avec IC à95% de de 2,12 à 3,51)
-
-
-
- ARA-NSel/Glifz : OR de 3,87 (avec IC à 95% de 1,66 à 9,48)
-
-
-
- l’analyse du rang des différentes classes thérapeutiques : les gliflozines sont classées au premier rang pour chacun des critères de jugement primaire ou secondaires (méthode SUCRA) (8).
- les comparaisons indirectes significatives sont :
Conclusions des auteurs
Dans cette méta-analyse en réseau, l’utilisation des gliflozines ou des ARA-non stéroïdiens, en plus d’un IEC ou d’un sartan, est associée à une réduction des évènements d’un critère rénal composite et des hospitalisations pour décompensation cardiaque, cela chez des patients diabétiques de type 2 avec atteinte rénale, en comparaison à un placébo ou une absence de traitement. Les gliflozines, comparées aux ARA-non stéroïdiens, sont associées à un moindre risque d’hospitalisation pour décompensation cardiaque. L’utilisation des gliflozines est associée à une moindre mortalité globale.
Financement de l’étude
Non mentionné.
Conflit d’intérêt des auteurs
Les auteurs déclarent n’avoir aucun conflit d’intérêt.
Discussion
Evaluation de la méthodologie
La méthodologie de cette méta-analyse en réseaux est méticuleusement décrite, et statistiquement sophistiquée. Les stratégies de recherche et de sélection des études sont décrites en détails et suivent les recommandations PRISMA adaptées aux méta-analyses en réseau. Les différentes étapes du processus ont été réalisées de manière indépendante par deux chercheurs. Un troisième investigateur est intervenu en cas de désaccord. Notons cependant que la recherche s’est limitée aux études en anglais. Les risques de biais sont analysés avec précision. Une évaluation claire de la confiance dans chacun des résultats est faite. Les chercheurs ont pris beaucoup de précaution pour éviter les doublons de données et ont contacté les auteurs des études originales en cas de doute. Les 17 modèles étudiés sont à effet fixe, peu hétérogènes. Cependant, aucun des réseaux analysés n’étant en boucle fermée, les valeurs de preuve des comparaisons indirectes sont diminuées, l’inconsistance (transférabilité) ne pouvant être testée. Enfin, la méthode SUCRA (classement chiffré des différents traitements) ne peut qu’être indicative, particulièrement parce qu’elle ne permet pas d’apprécier la variabilité (13).
Interprétation des résultats
L’avantage d’une méta-analyse en réseau(x) est surtout d’évaluer les preuves indirectes.
Pour le critère primaire, la comparaison indirecte est faite entre deux bras rassemblant 4 études sur 16 (donc 25% des études) et 89% des patients (2 études concernent la finérénone ( un ARA non stéroïdien récemment commercialisé en Belgique), une étude la canagliflozine et une étude la dapagliflozine, regroupées en « gliflozines »). Elle est non significative.
Pour le critère secondaire « hospitalisation pour décompensation cardiaque », la comparaison indirecte - faite au départ des mêmes 4 études - est significative, en défaveur de la finérénone. Un argument fort diminue la confiance que nous pourrions avoir dans ce résultat : les patients des deux bras sont profondément différents : micro-albuminurie pour le bras finérénone, macro-albuminurie pour le bras « gliflozines », ce qui diminue fortement la transférabilité, fondamentalement nécessaire pour cette comparaison indirecte (14).
Le classement de molécules sur la base d’effets indésirables estimés sur des RCTs est toujours sujet à caution (15,16). Les chiffres publiés dans cette MA sont donc considérés comme purement indicatifs. Les effets indésirables des gliflozines sont bien connus des cliniciens : excès d’amputations, acido-cétoses, infections génitales (y compris gangrène de Fournier), hypotension orthostatique (17). Les effets indésirables de la finérénone et de ses analogues comprennent au moins l’hypotension, l’hyperkaliémie et l’hyponatrémie.
Enfin, les critères de sélection des RCTs aboutit ici à un patchwork de réseaux, avec de multiples critères de jugement, ce qui diminue encore la valeur accordée aux preuves : la sophistication statistique ne sauvera jamais des sources médiocres (garbage - in, garbage - out). Au total, cette méta-analyse en réseau, qui n’est pas un modèle de médecine factuelle, a le mérite d’attirer l’attention sur le concept d’inflammation et de nécrose médiées par le récepteur de l’aldostérone notamment au niveau rénal (18), et sur la nouvelle classe des antagonistes non stéroïdiens des récepteurs de l’aldostérone.
Que disent les guides de pratique clinique ?
La mise à jour la plus récente vient d’être publiée (19) ; outre les gliflozines, la finérénone est ajoutée comme traitement possible pour la prévention de l’aggravation de l’insuffisance rénale du patient diabétique de type 2, déjà traité par IEC ou sartan.
Conclusion de Minerva
Les auteurs de cette méta-analyse en réseau classent les gliflozines préférentiellement à la finérénone dans le traitement de l’insuffisance rénale du patient diabétique de type 2 déjà traité par IEC ou sartan. Les limites de cette étude ne permettent pas cette assertion de classement : les preuves d’efficacité portent pour la finérénone, sur des patients micro-albuminuriques, mais pour la canagliflozine et la dapagliflozine sur des patients macro-albuminuriques.
Leur prescription éventuelle doit tenir compte d’effets indésirables éventuellement sévères : hyponatrémie, hyperkaliémie, hypotension pour la finérénone ; excès d’amputations, acido-cétoses, infections génitales (y compris gangrène de Fournier), hypotension orthostatique pour les gliflozines.
- Verpooten GA. IEC et antagonistes des récepteurs de l’angiotensine II : rénoprotecteurs ? MinervaF 2007;6(1):4-6.
- Casas JP, Chua W, Loukogeorgakis S et al. Effect of inhibitors of the renin-angiotensin system and other antihypertensive drugs on renal outcomes: systematic review and meta-analysis. Lancet 2005;366:2026-33. DOI: 10.1016/S0140-6736(05)67814-2
- Vanhaeverbeek M. Les inhibiteurs des SGLT2 (gliflozines) ont-ils un rôle en prévention primaire ou secondaire d’événements cardiovasculaires ou rénaux chez les patients diabétiques de type 2 ? Minerva Analyse15/06/2021.
- Zelniker TA, Wiviott SD, Raz I, et al. SGLT2 inhibitors for primary and secondary prevention of cardiovascular and renal outcomes in type 2 diabetes: a systematic review and meta-analysis of cardiovascular outcome trials. Lancet 2019;393:31-9. DOI: 10.1016/S0140-6736(18)32590-X
- Vanhaeverbeek M. La canagliflozine a-t-elle un effet freinateur sur l’évolution d’une néphropathie existante chez le patient diabétique de type 2 ? Minerva Analyse 15/09/2020.
- Perkovic V, Jardine MJ, Neal B, et al. Canagliflozin and renal outcomes in type 2 diabetes and nephropathy. N Engl J Med 2019;380:2295-306. DOI: 10.1056/NEJMoa1811744
- Wens J. L’empagliflozine prévient-elle la néphropathie chez les patients atteints de diabète de type 2 ? Minerva Analyse 15/12/2016.
- Wanner C, Inzucchi SE, Lachin JM, et al. Progression of kidney disease in type 2 diabetes. N Engl J Med 2016;375:323-34. DOI: 10.1056/NEJMoa1515920
- Lemiengre M. Insuffisance cardiaque gauche : importance des antagonistes de l’aldostérone. Minerva Analyse 28/08/2011.
- Ezekowitz JA, McAlister FA. Aldosterone blockade and left ventricular dysfunction: a systematic review of randomized clinical trials. Eur Heart J 2009;30:469-77. DOI: 10.1093/eurheartj/ehn543
- Kolkhof P, Bärfacker L. 30 Years of the mineralocorticoid receptor: mineralocorticoid receptor antagonists: 60 years of research and development. J Endocrinol 2017;234:T125-T140. DOI: 10.1530/JOE-16-0600
- Yang S, Zhao L, Mi Y, He W. Effects of sodium-glucose cotransporter-2 inhibitors and aldosterone antagonists, in addition to renin-angiotensin system antagonists, on major adverse kidney outcomes in patients with type 2 diabetes and chronic kidney disease: a systematic review and network meta-analysis. Diabetes Obes Metab 2022;24:2159-68. DOI: 10.1111/dom.14801
- Salanti G, Ades AE, Ioannidis JP. Graphical methods and numerical summaries for presenting results from multiple-treatment meta-analysis: an overview and tutorial. J Clin Epidemiol 2011;64:163-71. DOI: 10.1016/j.jclinepi.2010.03.016
- Rouse B, Chaimani A, Li T. Network meta-analysis: an introduction for clinician. Intern Emerg Med 2017;12:103-11. DOI: 10.1007/s11739-016-1583-7
- Sawchik J, Hamdani J, Vanhaeverbeek M. Randomized clinical trials and observational studies in the assessment of drug safety. Rev Epidemiol Sante Publique 2018;66:217-25. DOI: 10.1016/j.respe.2018.03.133
- Qureshi R, Mayo-Wilson E, Li T. Harms in systematic reviews Paper 1: An introduction to research on harms. J Clin Epidemiol 2022;143:186-96. DOI: 10.1016/j.jclinepi.2021.10.023
- Rédaction Prescrire. Effets secondaires des gliflozines. Rev Prescrire 2021;41:684-5.
- Epstein M. Aldosterone and mineralocorticoid receptor signaling as determinants of cardiovascular and renal injury: from Hans Selye to the present. Am J Nephrol 2021;52:209-216. DOI: 10.1159/000515622
- Zhang RM, Persson F, McGill JB, Rossing P. Clinical implications and guidelines for CKD in type 2 diabetes. Nephrol Dial Transplant 2023;38:542-50. DOI: 10.1093/ndt/gfac285
Auteurs
Vanhaeverbeek M.
Laboratoire de Médecine Factuelle, Faculté de Médecine, ULB
COI : Absence de conflits d’intérêt avec le sujet.
Mots-clés
antagoniste des récepteurs des minéralocorticoïdes, diabète de type 2, gliflozine, hospitalisation, hyperkaliémie, hyponatrémie, infarctus du myocarde, inhibiteur du SGLT2, insuffisance cardiaque, insuffisance rénale chronique, mortalité, mortalité cardiovasculaire, placebo, pression artérielleGlossaire
Code
Ajoutez un commentaire
Commentaires