Revue d'Evidence-Based Medicine
Biais du temps d’avance au diagnostic et biais de sélection des cancers les plus favorables
| La rédaction consacre une rubrique ‘Formation médicale continue’ (FMC) à l’explicitation de concepts et outils en Evidence-Based Medicine (EBM) |
Lorsque l’on veut dépister précocement un cancer par dépistage systématique, on peut, lors de la détermination de la survie, faire deux fautes systématiques. La première faute (biais du temps d’avance au diagnostic) est l’impression d’une plus longue survie alors qu’il ne s’agit que d’un diagnostic plus précoce et d’une durée de maladie plus longue pour le patient. Une deuxième faute (biais de sélection des cancers les plus favorables) est la conséquence d’une sélection par le dépistage de tumeurs à croissance plus lente avec une survie naturellement meilleure ce qui fait que la survie plus longue est moins la conséquence du dépistage que la suite de la sélection de tumeurs avec un meilleur pronostic.
Biais du temps d’avance au diagnostic
Le cancer est une maladie avec différents stades. Le départ est une cellule qui dégénère, le stade final est le décès par extension locale ou métastases. Quelque part dans le cours de ce processus le patient se présente chez le médecin avec un symptôme, des crachats sanglants, une douleur abdominale, des difficultés urinaires, une grosseur qui n’existait précédemment pas. Le diagnostic est posé un court ou un long moment ensuite.
Le but du dépistage est d’avancer le point du diagnostic avant le stade auquel les symptômes cliniques se développent. En cas de cancer, les symptômes apparaissent généralement suite à la croissance locale ou à cause du retentissement sur une fonction vitale. La rationalité du dépistage du cancer est que la découverte du cancer à un stade plus précoce équivaut à la découverte d’un petit cancer avec des possibilités de traitements plus efficientes.
Figure 1

La figure trace la ligne de vie théorique pour un patient cancéreux. Au point a survient une dégénérescence maligne d’une cellule. Durant la première période de croissance locale, la lésion est généralement trop petite pour être découverte par un test. A partir du point b, la tumeur devient bien détectable par un test de dépistage approprié. La rapidité d’apparition du b après le a dépend du type de cancer et de la méthode de dépistage utilisée. Le cancer du col de l’utérus se développe dans la zone de transition entre l’épithélium glandulaire simple mucosecrétant et l’épithélium malpighien exocervical (non kératinisé). La technique de dépistage utilisée consiste à gratter des cellules au niveau de cette jonction au moyen d’une petite brosse ou d’une spatule. Cette méthode équivaut à un examen direct et le point b doit ici sans doute être relativement proche du point a. Lors du dépistage du cancer du sein, l’autoexamen par les femmes permet de trouver en général des tumeurs d’environ un centimètre cube. La mammographie, un examen aussi indirect, permet de trouver des cancers qui échappent à la sensibilité de mains même bien expérimentées. La qualité de la méthode fait se déplacer le point b dans la direction du point a.
Si vous pouvez monter dans un bus toutes les 10 minutes à un point déterminé, alors vous le verrez parfois passer sous votre nez et parfois il arrivera en même temps que vous mais la durée moyenne d’attente des passagers sera de cinq minutes.
Figure 2

Pour le dépistage, il en va de même. La population à risque que l’on va rechercher se trouvera toujours entre b (détectable) et c (symptomatique) mais en moyenne le temps entre le moment du dépistage et le moment où les symptômes pourraient apparaître sera la moitié de la phase préclinique de détection. Cette période de temps depuis le dépistage (s) jusqu’au moment où les symptômes devraient théoriquement se manifester (c) est appelé temps d’avance au diagnostic.
Un biais de temps d’avance au diagnostic est donc une falsification des résultats par le temps d’avance au diagnostic quand on compare la survie d’une population dépistée avec la survie d’une population non dépistée choisie comme groupe contrôle. Le temps d’avance au diagnostic moyen peut être calculé en déterminant l’incidence des nouvelles lésions trouvées lors de sessions immédiatement successives de dépistage. En ajoutant cette période à la survie dans le groupe contrôle on neutralise l’effet du temps d’avance au diagnostic. Si on ne le fait pas, alors l’effet du dépistage est surestimé (Garmyn 2012).
Biais de sélection des cancers les plus favorables
Figure 3
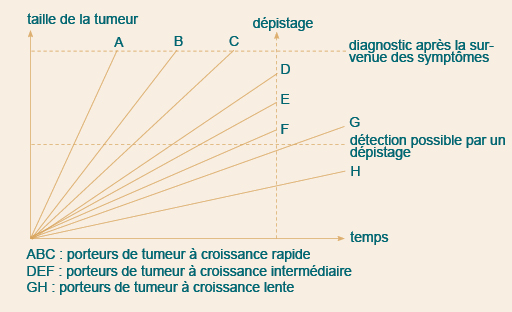
Nous savons que des tumeurs issues d’un même tissu se comportent quand même biologiquement différemment. Grosso modo, on distingue des porteurs de tumeurs à croissance rapides (ABC) et des porteurs de tumeurs à croissance lente (DEFGH). L’intervalle entre les séquences de dépistage détermine le nombre de porteurs de tumeur à croissance rapide qui seront dépistés dans la phase préclinique de détection (entre le point b et le point c). On choisit l’intervalle de dépistage en fonction d’un bénéfice supposé en années de vie, de la praticabilité, du coût et de la limitation des conséquences négatives du dépistage (fardeau psychologique, faux positifs). Les porteurs de tumeurs à croissance rapide A, B, C manifestent leur tumeur durant l’intervalle entre les dépistages ; ce sont des tumeurs dites d’intervalle. Pour les porteurs de tumeurs à croissance intermédiaire D, E et F, le dépistage les rend apparentes avant leurs manifestations cliniques. Les porteurs de tumeurs à croissance lente G et H ne peuvent être détectés lors du dépistage, le seuil de dépistage n’étant pas atteint. Un dépistage devrait donc sélectionner des tumeurs moins agressives, avec un pronostic naturellement meilleur et ceci à un stade plus précoce. L’effet falsifiant de ceci sur les résultats des études comparant la survie entre des personnes dont la tumeur est détectée lors d’un dépistage et un groupe contrôle avec des personnes chez lesquelles la tumeur est confirmée quand elle se manifeste cliniquement est appelé biais de sélection des cancers les plus favorables. On peut ici corriger quand on connaît la survie de porteurs de tumeurs à croissance rapide et qu’on compare celle-ci avec la survie de porteurs de tumeurs à croissance lente. Ces données sont aussi issues d’études descriptives et ici aussi des facteurs confondants non connus fournissent les biais nécessaires.
Références
Fletcher RH, Fletcher SW, Wagner EH. Clinical epidemiology, the essentials. Lippincott Williams & Wilkins. Baltimore. Fourth Edition 2005.
Greenberg RS, Daniels SR, Flanders WD, et al. Medical Epidemiology. Norwalk, Appleton and Lange, 1996.
Vandenbroucke JP, Hofman A, eds. Grondslagen der epidemiologie. Bunge 1993, p. 64-8.
Garmyn B. Quelle est l’efficacité du dépistage du cancer du sein à long terme (29 ans) ? MinervaF 2012;11(3):30-1.
Auteurs
Lemiengre M.
Huisartsenpraktijk De Wijngaard Roeselare; Vakgroep Huisartsgeneeskunde en Eerstelijnsgezondheidszorg, UGent
COI :
Glossaire
biais du temps d’avance au diagnosticCode
Ajoutez un commentaire
Commentaires





