Revue d'Evidence-Based Medicine
Comment exclure une TVP en première ligne de soins ?
Résumé
Contexte
En utilisant des données récoltées auprès de patients de deuxième ligne de soins, Wells et collaborateurs ont développé un score permettant d’évaluer le risque de la présence d’une TVP (1,2). L’applicabilité de ce score dans un contexte de première ligne de soins, chez des patients avec suspicion de TVP n’avait pas été évaluée.
Population étudiée
- région des Pays-Bas : population de 250 000 habitants ; 110 médecins traitants (100% de participation à l’étude) ; 3 hôpitaux
- critères d’inclusion : patients >18 ans chez lesquels le médecin traitant suspecte la présence d’une TVP en raison du gonflement, de la rougeur ou d’une douleur au niveau d’une jambe depuis ≤30 jours
- critères d’exclusion : patients avec suspicion d’embolie pulmonaire
- participants : 1 295 patients de 60 ans (ET 17) d’âge moyen.
Protocole d’étude
- les médecins traitants enregistrent sur un formulaire standardisé : anamnèse, signes cliniques et les 9 éléments du score de Wells (voir tableau 2)
- mais aussi une évaluation du risque de TVP :
- TVP fort probable ; pas de diagnostic alternatif
- TVP moins probable ; diagnostic alternatif possible
- TVP peu probable ; diagnostic alternatif certain
- en cas de risque de TVP jugé moins ou peu probable, retrait de 2 points du score positif ; score ≤0 risque bas, score 1 à 2 risque modéré, score ≥3 risque élevé
- tous les patients sont référés pour une échographie avec compression (avec examinateur en insu) et détermination des D-dimères hautement sensibles ; une échographie avec compression protocolée normale est répétée après 7 jours ; une échographie anormale confirme le diagnostic.
Mesure des résultats
sensibilité, spécificité, valeur prédictive négative et rapport de vraisemblance négatif.
Résultats
- pour le score de Wells, 39% des patients ont un risque faible, 25% un risque modéré et 36% un risque élevé de TVP
- la prévalence, sur base de l’échographie avec compression est estimée à 22% : 12% dans le groupe à bas risque, 16,5% dans le groupe à risque modéré et 37,5% dans le groupe à haut risque
- en prenant la valeur la plus basse (≤0) du score de Wells comme seuil versus les deux valeurs les plus hautes (≥1), la sensibilité de ce score est de 78,9% (IC à 95% de 74 à 84), la spécificité de 44,3% (41 à 47), la valeur prédictive négative de 88,0% (85 à 91) et le rapport de vraisemblance négatif de 0,48 (0,38 à 0,60)
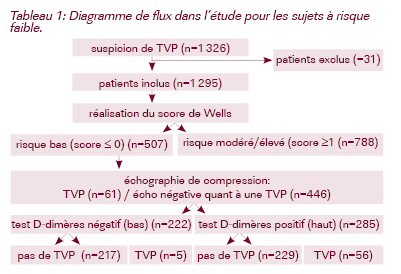
- en associant le score de Wells obtenu aux résultats du dosage des D-dimères, l’efficacité du test est accrue pour exclure une TVP : sensibilité de 98% (97 à 100), spécificité de 22% (19 à 24), valeur prédictive négative de 98% (96 à 100) et rapport de vraisemblance négatif de 0,08 (0,03 à 0,19) ou force excluante de 12,5 (bonne) ; cette association de tests loupe 2,3% des TVP (voir tableau 1 pour diagramme de flux dans l’étude, pour les sujets à risque faible).
Conclusion des auteurs
Les auteurs concluent que le score de Wells à lui seul ou associé à un dosage des D-dimères ne garantit pas une évaluation précise du risque de TVP chez des patients se présentant en première ligne de soins avec une suspicion de TVP.
Financement
Stichting Gezondheidszorg Onderzoek “IJsselmond” Zwolle, Nederland et ZonMw.
Conflits d’intérêt
Aucun n’est mentionné.
Discussion
Discussion des résultats
L’évaluation de l’efficacité du score de Wells dans l’évaluation du risque a priori de présence d’une TVP s’est limitée, avant cette étude, à des patients se présentant à l’hôpital (1,2). La différence la plus importante entre les résultats de cette étude et celles de Wells, est la prévalence des TVP dans les différentes cohortes. Pour les scores les plus bas, Oudega et coll. observent un chiffre de 12% ce qui est 4 fois supérieur à la valeur observée dans l’étude de Wells. Cette importante différence de prévalence en TVP entre la médecine de famille et l’hôpital peut-elle être expliquée ? Une sélection plus rigoureuse est-elle opérée ? C’est la haute prévalence de TVP qui explique qu’un rapport de vraisemblance négatif pour l’association des tests (Wells + D-dimères) à 0,08 s’accompagne malgré tout d’un nombre inacceptablement élevé (2,3%) de faux négatifs. Il s’agit, en effet, d’une affection à risque vital.
Considérations sur la méthodologie
Oudega et collaborateurs permettent aux médecins traitants d’évaluer le risque a priori. Ceux-ci ont scrupuleusement respecté leur mission, chaque médecin traitant incluant en moyenne plus de dix patients. Une étude effectuée dans un contexte semblable en Nouvelle-Zélande a inclus moins d’un patient par médecin de famille (3). Ce sont les deux seules études qui ont évalué une classification des patients au moyen du score de Wells par des généralistes. C’est la force mais aussi la faiblesse de l’étude. Au sein d’un hôpital, les membres du personnel qui incluent des patients dans une étude peuvent acquérir une formation plus importante et être éventuellement supervisés ; le nombre de médecins différents utilisant le score est également nettement moindre ce qui peut faire l’épargne d’un biais interobservateur, biais qui a probablement joué un rôle important dans l’étude analysée ici. L’âge moyen de la cohorte observée est légèrement plus élevé que celui de la cohorte évaluée par Wells (60 vs 57 ans). La méta-analyse de Goodacre (4) suggère que le score de Wells est moins performant chez les patients âgés de plus de 60 ans (rapport de vraisemblance négatif à 0,30 par rapport à un chiffre de 0,24 chez des patients plus jeunes). Oudega modifie également le score de Wells en substituant à une question (« Existe-t-il un diagnostic alternatif au moins aussi probable qu’une TVP ? ») une autre question proposant trois catégories de réponses, afin d’éviter un biais interobservateur. Wells opte également pour un diagnostic de référence de TVP basé sur une échographie avec compression unique et un examen de suivi après 3 mois. L’échographie avec compression est-elle un gold standard bien établi ? Oudega choisit de répéter l’échographie après une semaine en cas de résultat initial négatif. Un suivi plus important, de trois mois, aurait sans doute gonflé le numérateur et accentué les différences par rapport à l’étude de Wells. Wells exclut les patients ayant déjà présenté une TVP, ce qui est une autre explication possible pour l’incidence plus élevée enregistrée par Oudega qui n’exclut pas de tels patients (1). Oudega a cependant recalculé la prévalence de TVP chez les patients sans anamnèse de TVP et obtient des résultats similaires en pourcentage.
Score d’Oudega
En exploitant les données de son étude de cohorte, Oudega a élaboré un nouveau score diagnostique pour exclure une TVP, en recourant à 8 items qui, positifs, augmentent la valeur obtenue au score (voir tableau 2). En appliquant ce score à sa cohorte de recherche et en fixant une valeur seuil à ≤ 3 points, la prévalence de TVP dans ce groupe est encore de 0,7%, ce qui signifie une sensibilité de 99,3% (IC à 95% de 98,4 à 100), une spécificité de 28,9% (26,1 à 31,7) et un rapport de vraisemblance négatif de 0,02. Ce test n’a malheureusement pas été évalué dans d’autres types de population (5,6).
Tableau 2

Conclusion
Cette étude montre que le score de Wells associé ou non à un dosage des D-dimères, utilisé par des médecins généralistes en première ligne de soins, est insuffisamment précis pour identifier des patients avec un risque de TVP a priori < 3%. Différentes études incluant des patients se présentant dans des services d’urgence hospitaliers avaient, par contre, montré son intérêt. Chez des patients à risque de TVP a priori bas, il faut mesurer les D-dimères (avec un test à haute sensibilité), et si ce test est négatif, une TVP peut être exclue. Chez des patients avec un risque de TVP a priori moyen ou élevé, une échographie avec compression des membres inférieurs est l’étape diagnostique suivante (7-9).
Références
- Wells PS, Anderson DR, Bormanis J, et al. Value of assessment of pretest probability of deep vein thrombosis in clinical management. Lancet 1997;350:1795-8.
- Wells PS, Anderson DR, Rodger M, et al. Evaluation of D-dimer in the diagnosis of suspected deep-vein thrombosis. N Engl J Med 2003;349:1227-35.
- Maelen T, Raina C. Accuracy of the Wells rule in diagnosing venous thrombosis in primary health care. N Z Med J 2007;120:U2705.
- Goodacre S, Sutton AJ, Sampson FC. Meta-analysis: The value of clinical assessment in the diagnosis of deep venous thrombosis. Ann Intern Med 2005;143:129-39.
- Oudega R, Moons KG, Hoes AW. Ruling out deep venous thrombosis in primary care. A simple diagnostic algorithm including D-dimer testing. Thromb Haemost 2005;94:200-5.
- Toll DB, Oudega R, Bulten RJ, et al. Excluding deep vein thrombosis safely in primary care. J Fam Pract 2006;55:613-8.
- Qasseem A, Snow V, Barry P, et al; Joint American Academy of Family Physicians/American College of Physicians Panel on Deep Venous Thrombosis/Pulmonary Embolism. Current diagnosis of venous thromboembolism in primary care: a clinical practice guideline from the American Academy of Family Physicians and the American College of Physicians. Ann Fam Med 2007;5:57-62.
- Lemiengre M, Vanhee L. Intérêt du test D-Dimères lors d’une suspicion de TVP. MinervaF 2005;4(4):52-4.
- Lemiengre M, Vanhee L. Quel est le test D-Dimères le plus performant pour exclure une TVP ou une embolie pulmonaire ? MinervaF 2005;4(4):58-60.
Auteurs
Lemiengre M.
Huisartsenpraktijk De Wijngaard Roeselare; Vakgroep Huisartsgeneeskunde en Eerstelijnsgezondheidszorg, UGent
COI :
Code
Ajoutez un commentaire
Commentaires





